Транзиторная иммунная недостаточность можно ли делать прививки
Содержание статьи
Вакцинация лиц с иммунодефицитом | Компетентно о здоровье на iLive
Общие правила вакцинации лиц с иммунодефицитом
У больных с иммунодефицитом полностью безопасны инактивированные вакцины. Живые вакцины в принципе противопоказаны, хотя ВИЧ-инфицированным их вводят.
Первичные иммунодефицитные состояния
Повышенный риск осложнений для этих больных доказан в отношении живых вакцин. Это вакцино-ассоциированный полиомиелит (ВАП) при применении ОПВ и энцефалит в ответ на коревую вакцину у лиц с а- и гипогаммаглобулинемией, генерализованный БЦЖ-ит и БЦЖ-остеит у детей комбинированными формами иммунодефицита, с хронической гранулематозной болезнью и дефектами в системе интерферона-у и интерлейкина 12. Клинические проявления иммунодефицита отсутствуют у новорожденных, когда вводят БЦЖ, а чаще всего и возрасту 3 месяцев, когда вводили ОПВ (это связано с компенсацией материнскими IgG недостаточности собственных иммуноглобулинов); по этой причине поголовное исследование детей первых месяцев на наличие иммунодефицита не информативно, да и практически нереально.
Иммунизация живыми вакцинами лиц с иммунодефицитом
Вид иммунодефицита | Сроки введения живых вакцин |
Первичные иммунодефициты | Живые вакцины не вводят, ОПВ заменяют на ИПВ |
Подавляющие иммунитет болезни (опухоли, лейкоз) | Живые вакцины вводят в ремиссии в индивидуальные сроки |
Иммуносупрессия, лучевая терапия | Не ранее, чем через 3 месяца после окончания терапии |
Кортикостероиды (дозы указаны по преднизолону) | |
Внутрь >2 мг/кг/сут (>20 мг/сут при весе выше 10 кг) более 14 дней | Через 1 мес. после окончания курса |
Та же доза менее 14 дней или доза менее 2 мг/кг/сут ( | Сразу по окончании лечения |
Поддерживающее лечение | На фоне проводимого лечения |
Местная терапия (капли в глаза, нос, ингаляции, спреи и мази, в сустав) | На фоне проводимого лечения |
ВИЧ — инфекция | |
Бессимптомная — при отсутствии лабораторных признаков иммунодефицита | Коревая, паротитная, краснушная — с контролем антител через 6 мес. и повторной прививкой в случае их низкого уровня |
С признаками иммунодефицита | Защиту осуществляют иммуноглобулином |
Состояниями, заставляющими думать о возможности первичного иммунодефицита (у подлежащего вакцинации или у члена семьи) являются:
- тяжелое, особенно рецидивирующее гнойное заболевание;
- парапроктит, аноректальный свищ;
- наличие упорного кандидоза полости рта (молочницы), других слизистых и кожи;
- пневмоцистная пневмония;
- упорная экзема, в том числе себорейная;
- тромбоцитопения;
- наличие в семье больного иммунодефицитом.
У детей с такими состояниями надо определить содержание 3 классов иммуноглобулинов, иммунодефицит вероятен при снижении уровней иммуноглобулинов хотя бы одного класса ниже нижней границы нормы. Позволяет заподозрить гуморальный иммунодефицит снижение доли у-глобулинов ниже 10% в белковых фракциях крови. Для оценки состояния Т-клеточного дефицита используют кожные пробы с туберкулином (У вакцинированных БЦЖ) и кандидином — выпадение отрицательных проб требует Дальнейшего исследования. Диагноз хронической гранулематозной болезни подтверждают пробой с тетразолием синим или аналогичными.
БЦЖ не вводят новорожденным, в семье которых есть дети с любыми признаками Иммунодефицита, или дети, погибшие от нерасшифрованной патологии.
Для защиты детей с первичным иммунодефицитом от кори в случае контакта с больными используют иммуноглобулин человека (эти дети обычно получают заместительную терапию иммуноглобулином, который защищает их от заражения).
Детей с первичным иммунодефицитом вакцинируют всеми инактивированными вакцинами, в том числе на фоне заместительной терапии иммуноглобулином. Поскольку многие из них дают сниженный иммунный ответ, желательно определение титров антител по окончании первичной серии вакцинации и введение дополнительных доз при необходимости. Ответ на дифтерийный и столбнячный анатоксины полностью отсутствует у детей с гипер-IgE синдромом, синдромах дефицита антител.
Влияние иммуносупрессии на уровни антител
Инфекция | Сохранение антител | |
Постинфекционные | Поствакцинальные | |
Столбняк | сохранены | |
Дифтерия | сохранены | |
Полиомиелит | сохранены | |
Корь | снижены | |
Пневмококковая | сохранены (лимфомы) | |
Ветряная оспа | снижены | |
Гепатит В | снижены | |
Грипп | снижены | |
Транзиторная гипогаммаглобулинемия
Этот так называемый «поздний иммунологический старт» обычно проходит к 2-4 годам, таких детей можно прививать убитыми вакцинами, а после нормализации иммуноглобулинов вакцинировать от кори, краснухи и паротита. БЦЖ эти дети переносят обычно.
Ассоциированный с болезнями иммунодефицит и иммуносупрессивная терапия
Иммунный ответ подавлен при лейкозах, лимфогранулематозе и других лимфомах, в несколько меньшей степени при ряде солидных опухолей; это является противопоказанием для введения живых вакцин, тем более, что эти дети обычно получают иммуносупрессивную терапию. Хотя введение им убитых вакцин в остром периоде не противопоказано, иммунный ответ на ряд вакцин бывает часто снижен:
- На дифтерийный и столбнячный анатоксина ответ хороший (на бустерную дозу), хуже на первичную серию.
- Хиб-вакцина вызывает обычно хороший ответ.
- Ответ на Гриппол не снижается, но в дошкольном возрасте требуется 2 дозы.
- Гепатитная В вакцина — иммунный ответ крайне слабый.
По этой причине ряд вакцин рекомендуется вводить не ранее, чем через 4 недели после окончания терапии (при числе лимфоцитов более 1000 в 1 мкл). Живые вакцины вводят индивидуально, минимум через 3 мес. после окончания иммуносупрессии.
У детей с острым лимфобластным лейкозом при контакте с ветряной оспой (или опоясывающим лишаем, часто обостряющимся у перенесших ветряную оспу соседеи по палате) необходимо прерывать курс химиотерапии, профилактически применять ацикловир, возможно также применить в/в иммуноглобулин человека. Надежнее зашита достигается вакцинацией, рекомендованная ВОЗ и широко проводимая в мире: она предотвращает заболевание у 85% больных, у остальных инфекция протекает легко. У болевших ранее вакцинация, действуя как бустер, снижает частоту обострений опоясывающего лишая. Больных лейкозом прививают через 1 год ремиссии на фоне поддерживающей терапии при числе лимфоцитов не менее 700 в 1 мкл и тромбоцитов более 100 000 в 1 мкл. Вакцинация оказывается эффективной и у реципиентов трансплантатов костного мозга и солидных органов.
У больных лейкозом высок риск гепатита В в связи с повторными гемотрансфузиями. В настоящее время защиту этих больных от заражения гепатитом В осуществляют путем введения специфического иммуноглобулина, обычно в сочетании с активной иммунизацией на более поздней стадии лечения.
Больных лимфогранулематозом вакцинируют согласно указанным выше правилам. С учетом особой их восприимчивости к инфекциям, вызванным капсульными микроорганизмами, им рекомендуется также вводить Хиб-вакцину, а в возрасте старше 2 лет — вакцины против пневмококковой и менингококковой А и С инфекций. Вакцинацию следует проводить за 10-15 дней до начала очередного курса терапии или через 3 мес. и более после его окончания. Эта же тактика используется у детей с аспленией и нейтропенией, имеющих повышенный риск бактериемической инфекции капсульными микроорганизмами.
Иммуносупрессия снижает уровни антител, поэтому по выходе в ремиссию показана вакцинация (или ревакцинация) против дифтерии и столбняка, кори (даже после 1 или 2 прививок), краснухи и паротита, гриппа, гепатита В, ветряной оспы.
Детей после трансплантации костного мозга прививают убитыми вакцинами не менее чем через 6 мес, живыми вакцинами — через 2 года двукратно (интервал 1 мес.)
Иммунные дефекты, вызывающие повышенную восприимчивость к инфекции капсульными возбудителями (пневмококком, Н. influenzae типа b, менингококком). К ним относятся больные с аспленией (дефект образования IgM-антител), имеющих высокий риск пневмонии (заболеваемость 226 на 100 000 больных, ОР 20,5), который сохраняется десятилетиями после удаления селезенки. При серповидноклеточной анемии (функциональная аспления) в возрасте до 5 лет частота пневмококковой инфекции (6,9 на 100 человеко-лет) в 30-100 раз выше показателей заболеваемости всего населения. У больных диабетом пневмококковая инфекция, хотя и возникает не чаще, чем у здоровых, течет тяжело, с летальностью 17-42%.
Рецидивы менингококковой инфекции часты у лиц с дефицитом пропердина, С3 и ряда последующих компонентов комплемента, их рекомендуют прививать полисахаридной вакциной каждые 3 года.
Контроль за результатом вакцинации лиц с иммунодефицитом и иммуносупрессией путем определения титров соответствующих антител обязателен.
[1], [2], [3], [4], [5], [6], [7], [8], [9]
Кортикостероидная терапия
Стероиды приводят к выраженной иммуносупрессии лишь при использовании высоких доз (преднизолон >2 мг/кг/сут или >20 мг/сут для ребенка весом >10 кг) в течение более 14 дней. Таким детям убитые вакцины вводятся в обычные сроки по выздоровлении, живые вакцины вводят не ранее, чем через 1 месяц от окончания лечения. Живые и инактивированные вакцины вводятся в обычном порядке лицам, получающим стероидные препараты в виде:
- кратковременных курсов (до 1 недели) в любых дозах;
- курсами до 2 недель в низких или средних (до 1 мг/кг/сут преднизолона) дозах;
- длительно в поддерживающих дозах (например, 10 мг преднизолона через день);
- заместительной терапии в низких (физиологических) дозах;
- местно: накожно, в ингаляциях, в виде глазных капель, внутрь сустава.
[10], [11], [12], [13], [14], [15], [16], [17]
Источник
ранзиторные иммунодефициты. Механизм развития транзиторных иммунодефицитов. Иммунотерапия. Иммунопрофилактика. Иммунобиологические препараты.
Оглавление темы «Иммунодефициты. Вакцины. Сыворотки. Иммуноглобулины.»:
1. Клеточные иммунодефициты. Т-клеточная недостаточность иммунитета. Диагностика клеточных иммунодефицитов. Синдром Ди Джорджи. Синдром Незелофа. Тяжёлый комбинированный иммунодефицит. Синдром Вискотта-Олдрича.
2. Транзиторные иммунодефициты. Механизм развития транзиторных иммунодефицитов. Иммунотерапия. Иммунопрофилактика. Иммунобиологические препараты.
3. Виды иммунобиологических препаратов. Эффекты иммунобиологических препаратов.
4. Вакцины. Виды антигенов вакцин. Классификация вакцин. Виды вакцин. Живые вакцины. Ослабленные ( аттенуированные ) вакцины. Дивергентные вакцины.
5. Инактивированные вакцины. Корпускулярные ( цельновирионные ) вакцины. Компонентные ( субъединичные ) вакцины.
6. Генно-инженерные ( рекомбинантные ) вакцины. Векторные вакцины. Синтетические вакцины.
7. Молекулярные вакцины. Анатоксины. Классификация анатоксинов. Конъюгированные вакцины.
8. Моновалентные вакцины. Ассоциированные ( поливалентные ) вакцины. Методы вакцинопрофилактики. Методы введения вакцин. Типы вакцинаций. Виды вакцинаций.
9. Эффективность вакцин. Проверка эффективности вакцин. Индекс защиты вакцины. Индекс эффективности вакцины.
10. Сывороточные иммунные препараты. Иммунные сыворотки. Гетерологичные сыворотки. Гомологичные сыворотки. Иммунные иммуноглобулины.
Транзиторные иммунодефициты. Механизм развития транзиторных иммунодефицитов. Иммунотерапия. Иммунопрофилактика. Иммунобиологические препараты.
Многие инфекционные заболевания сопровождаются дефектами иммунной реактивности. Подобные нарушения известны ещё со времён фон Пирке (начало XX века), однако в большинстве случаев они носят временный характер и исчезают после выздоровления.
Основополагающий механизм развития транзиторных иммунодефицитов — повреждение или инфицирование иммунокомпетентных клеток с последующим нарушением их функций. Особенно часто транзиторные иммунодефицита наблюдают на фоне вирусных инфекций, что обусловлено облигатным внутриклеточным паразитизмом возбудителей. Наиболее яркий пример — ВИЧ, избирательно инфицирущий Т-хелперы. В результате развивается прогрессирующее разрушение иммунной системы — синдром приобретённого иммунодефицита (СПИД).
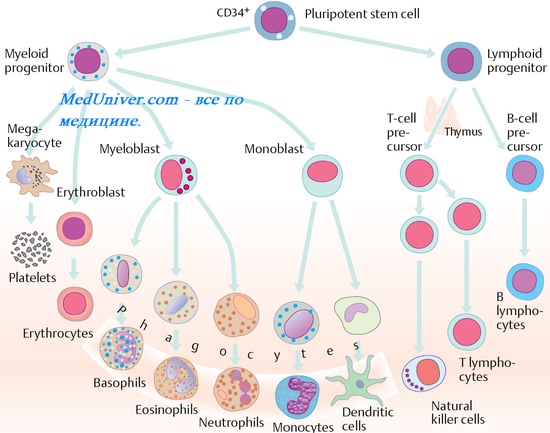
Иммунотерапия. Иммунопрофилактика. Иммунобиологические препараты
Иммунотерапия — введение с лечебными целями иммунных препаратов (например, AT, ИФН, цитокинов и др.). Иммунопрофилактика — введение иммунных препаратов с целью предотвращения развития инфекционных заболеваний (вакцины, сыворотки). На протяжении столетий практическая медицина применяла эмпирические методы искусственной защиты от инфекционных болезней (например, от оспы). Научные основы иммунопрофилактики были заложены исследованиями Пастера, открывшего феномен аттенуации (ослабления) микробов и создавшего вакцины против сибирской язвы и бешенства.
Все средства, применяемые для воздействия на иммунную систему, известны как иммунобиологические препараты. К ним относят разнообразные по природе и происхождению вещества.
— Также рекомендуем «Виды иммунобиологических препаратов. Эффекты иммунобиологических препаратов.»
Источник
Транзиторная иммунная недостаточность можно ли делать прививки — Всё о прививках
Транзиторная гиппогаммаглобулинемия – это форма иммунодефицита, который проявляется у детей, не достигших трехлетнего возраста. Это временное состояние детского организма, которое характеризуется снижением уровня антител в крови ребенка, его способности сопротивляться различного рода инфекциям и болезням. Также такое состояние характеризуется как поздний иммунологический старт, то есть пониженная способность организма бороться с вредными микроорганизмами и микробами, которая проявляется у детей грудного возраста и прекращается по достижению возраста двух-трех лет.
Причины:
- Недостаток антител, которые передаются ребенку с молоком матери.
- Незрелость иммунной системы, которая окончательно сформируется только к десяти годам жизни ребенка.
- Недостаток иммуноглобулина, который усваивается еще в утробе матери.
- Заболевания, связанные с иммунодефицитом у самих родителей.
Признаки
Заболевание диагностируется случайно, так как практически невозможно его выявить самостоятельно, из-за того, что симптомы схожи с течением многих респираторных и вирусных заболеваний. Кроме того, болезнь не является опасной и при употреблении достаточного количества необходимых организму белков и витаминов ребенок успешно с ней борется. Симптомы одинаково проявляются как у мальчиков, так и у девочек, поэтому выявить наличие болезни по половому признаку невозможно. Считается, что повышение частоты заболевания вирусными инфекциями у ребенка, достигшего возраста шести месяцев, и есть основной признак заболевания транзиторной гиппогаммаглобулинемией. Это могут быть и бронхит, и отит, то есть те инфекции, которые не угрожают жизни ребенка, но способствуют снижению иммунитета и ухудшению общего состояния организма. При этом лимфатические узлы и миндалины остаются в нормальном здоровом состоянии. Могут значительно пострадать почки, а также возможны различные гнойные заболевания, которые и возникают вследствие пониженного иммунитета.
Виды
Учеными-медиками выявлено несколько видов транзиторной гиппогаммаглобулинемии, среди которых можно выделить:
- Физиологическую гиппогаммаглобулинемию, которая характеризуется общей слабостью организма к сопротивлению вирусам и проходит по достижению ребенком полугода.
- Патологическая гиппогаммаглобулинемия. Проявляется в основном у недоношенных детей, так как у них не успела завершиться окончательная передача иммуноглобулина через плаценту, осуществляемая с двадцатой недели и вплоть до рождения ребенка. Данный вид заболевания может проявляться и у взрослых и носить врожденные либо приобретенные признаки. В этом случае повышается риск заболеваний различными вирусными инфекциями, так как организм не поучает достаточного количества иммуноглобулина. Врожденный иммунодефицит достаточно хорошо лечится у детей, тогда как у взрослых лечение затрудненно. Возникает риск врожденного иммунодефицита, когда таковой уже имеется у матери ребенка. Приобретенный иммунодефицит может стать следствием тяжелых заболеваний и операций, лечение которых сопровождалось приемом сильных лекарств, влияющих на понижение иммунитета.
Итак, среди перечисленных видов транзиторной гиппогаммаглобулемии наиболее опасным для здоровья является патологическая гиппогаммаглобулемия.
Диагностика
Точные признаки болезни выявить невозможно, поэтому считается, что болезнь имеет место быть, когда происходит снижение насыщенности крови одним либо несколькими изотопами иммуноглобулина, больше, чем на две единицы, характерные для определенного возраста. Но все остальное, в том числе и синтез специфических антител, соответствует возрасту и нормальной жизнедеятельности организма. Поэтому диагностировать болезнь сразу невозможно, а в некоторых случаях ни родители, ни сам ребенок не подозревают о болезни, которая с возрастом проходит сама.
Лечение
И все же при выявлении болезни назначается определенное лечение, которое может заключаться во введении внутривенно иммуноглобулина, но такое возможно только в очень тяжелых случаях протекания болезни. В остальных же случаях лечение вовсе не назначается и болезнь с возрастом проходит сама. Для выявления болезни возможны проведение следующих видов обследования:
- Проверка на наличие сывороточных иммуноглобулинов класса А, М и G. При этом иммуноглобулин А защищает слизистую оболочку человека, он тормозит все микробы во рту и не дает им проникнуть внутрь организма. Данный класс иммуноглобулина не обладает памятью на вирусы и каждый раз вырабатывает на них новые средства защиты. Таким образом, при проведении анализа, показавшего повышенный уровень иммуноглобулина А, можно с уверенностью сказать, что в организме происходит сильный воспалительный процесс, что уже наводит на мысль о возможности иммунодефицита. Иммуноглобулин класса М вырабатывается для борьбы с патогенами и также не обладает функцией запоминания. Его особенностью является тот факт, что при встрече с одним и тем же микробом он все же способен запомнить его и уничтожить. Когда наблюдается отсутствие иммуноглобулина М, теряется возможность делать прививку, так как суть прививки как раз и состоит в постепенном введении антител в организм, чтобы заставить иммуноглобулин М постоянно работать. И здесь также можно поставить диагноз иммунодефицита. Поэтому детям с пониженной концентрацией в организме иммуноглобулина М прививки противопоказаны, так как их организму просто нечего противопоставить даже ослабленным микроорганизмам. Иммуноглобулин класса G проявляется при появлении вирусов и микробов, которые он запоминает и постоянно побеждает. Особенность данного вида иммуноглобулина состоит в том, что он борется не только с теми микробами, которые поступили, но и с теми, которые находятся в организме долгое время. Таким образом даже те организмы, которым удалось проскользнуть мимо защитных механизмов двух предыдущих видов иммуноглобулина, оказываются ликвидированы иммуноглобулином G. Отсутствие в крови данного иммуноглобулина также является первым тревожным показателем к проведению дальнейших исследований.
- Для выявления дефицита иммунитета также берется анализ крови и мочи.
- Проводятся дополнительные исследования на наличие бактерий.
В основном, как уже упоминалось, длительное лечение не требуется даже при постановке диагноза, так как болезнь проходит сама, постепенно сопротивляемость организма повышается и количество вирусов и микробов способных нанести вред здоровью ребенка снижается. Но особо опасна данная болезнь у детей склонных либо уже больных ВИЧ, так как все симптомы в основном схожи, вот только простая транзиторная гиппогаммаглобулинемия проходит с возрастом, а диагноз иммунодефицита требует серьезного и длительного лечения. Поэтому следует сразу же разграничить эти два понятия и не пугаться поставленного диагноза, помня о том, что болезнь возрастная в отличие от ВИЧ.
Итак, транзиторная гиппогаммаглобулия болезнь недостатка иммунодефицита, которая проявляется у детей в младенческом возрасте и не оказывает значительного воздействия на организм не требует специального лечения и проходит самостоятельно, без рецидивов и летальных исходов.
Source: www.skalpil.ru
Источник