Можно ли есть перед неонатальным скринингом
Содержание статьи
Вопросы и ответы по первому скринингу

Определяют ли пол ребенка на первом скрининге?
Теоретически это можно сделать: срок уже позволяет. Однако будущий ребенок не всегда располагается так, чтобы врач с уверенностью назвал пол. Более достоверные сведения получают, начиная с шестнадцатой недели.
Каков срок первого скрининга?
Первый скрининг проводят в промежутке между 11-й и 14-й неделями беременности. Если исследование выполнено раньше этого срока, возможна неверная интерпретация данных. То же самое относится к информации, полученной после 14-й недели.
На что берут кровь при первом скрининге?
Анализ крови делают с целью установить уровень таких веществ, как β-ХГЧ и РАРР-А. Бета-хорионический гонадотропин важен для плода на ранних стадиях развития. В норме уровень этого гормонального вещества повышается, а затем плавно снижается.
Чрезмерно высокое содержание β-ХГЧ говорит об опасности синдрома Дауна. Эти показатели также характерны для раннего токсикоза, многоплодной беременности, сахарного токсикоза у матери. Если уровень бета-хорионического гонадотропина ниже нормы, возможны такие патологии, как:
- плацентарная недостаточность;
- внематочная беременность;
- синдром Эдвардса у плода.
Белковый протеин А необходим для правильного развития и работы плаценты. Повышенное содержание РАРР-А не вызывает тревогу, а вот снижение уровня указывает на угрозу самопроизвольного прерывания беременности и развитие синдромов де Ланге и Дауна.
Скрининг 1 триместра: сдавать кровь натощак или нет?
Кровь для исследования берут из вены. Поэтому приходить в процедурный кабинет необходимо натощак. Разрешается выпить немного чистой воды без газа.
Первый скрининг: какая нужна подготовка к сдаче крови?
Перед сдачей крови на бета-хорионический гонадотропин и протеин-А необходимо соблюдать ряд условий. Следует:
- за 2-3 дня отказаться от интимной близости;
- накануне исключить из меню жирное мясо, шоколад, морепродукты;
- ничего не есть за 6 часа до анализа.
Важно также находиться в спокойном состоянии, не нервничать, не ускорять шаг при ходьбе. Стресс и физическая активность способны вызвать повышение концентрации некоторых веществ в организме, что исказит результаты анализа.
Первый скрининг: что важнее — кровь или УЗИ?
Важны оба исследования. Они дополняют друг друга и позволяют получить более точную информацию.
Вначале необходимо сделать ультразвуковое исследование: оно точно определит срок беременности. Это позволит сравнить результаты анализа крови с показателями нормы, которые на ранних этапах развития плода меняются каждый день.
Что нельзя есть перед первым скринингом крови?
За 2-3 суток до двойного теста необходимо придерживаться специальной диеты. Это очень важно требование, поскольку его несоблюдение влечет за собой искажение результатов.
Перед скринингом крови нужно отказаться от:
- жареной и приправленной специями пищи;
- жирного мяса;
- мясопродуктов (колбасы, сала, бекона, копченостей);
- консервов.
Под запретом также находятся шоколад, орехи, куриные яйца, морепродукты, капуста, ржаной хлеб, бобовые.
Разрешены крупы, сливочное и растительное масло, макароны, мед, овощи в свежем и отварном виде. Из мясных блюд показана отварная курятина.
Какие анализы сдают в 1 триместре беременности?
При первичной постановке на учет, примерно на 4-6 неделях, назначают:
- общий анализ мочи и крови;
- биохимический анализ крови (из вены);
- тесты на гепатиты, ВИЧ, сифилис, ИППП, вирус простого герпеса, краснуху, цитомегаловирусную инфекцию, токсоплазмоз.
Следует также определить резус и группу крови, сделать коагулограмму.
Каждые четыре недели перед визитом к врачу-гинекологу нужно сдавать общий анализ мочи. Это позволяет контролировать состояние мочеполовой системы, выявить воспалительные заболевания, ранний токсикоз, гестационный сахарный диабет.
На 11-14 неделе будущая мама проходит первый скрининг. Один из его этапов — сдача крови на определение уровня протеина-А и бета-хорионического гонадотропина.
Статья проверена на соответствие медицинским стандартам ведущим специалистом клиники «Поликлиника+1», дерматовенерологом, урологом, микологом
Малашенко Владимиром Александровичем
Источник
Остановить болезнь до появления симптомов. Что такое неонатальный скрининг и зачем его проводить младенцам?
Около 5% всего населения имеют врожденные или наследственные заболевания. И хотя подавляющее большинство генетических болезней еще не имеет лечения, их диагностика очень сильно продвинулась вперед. Зачем проводить массовый скрининг и почему в России не проверяют младенцев на десятки заболеваний сразу, узнали «Такие дела».
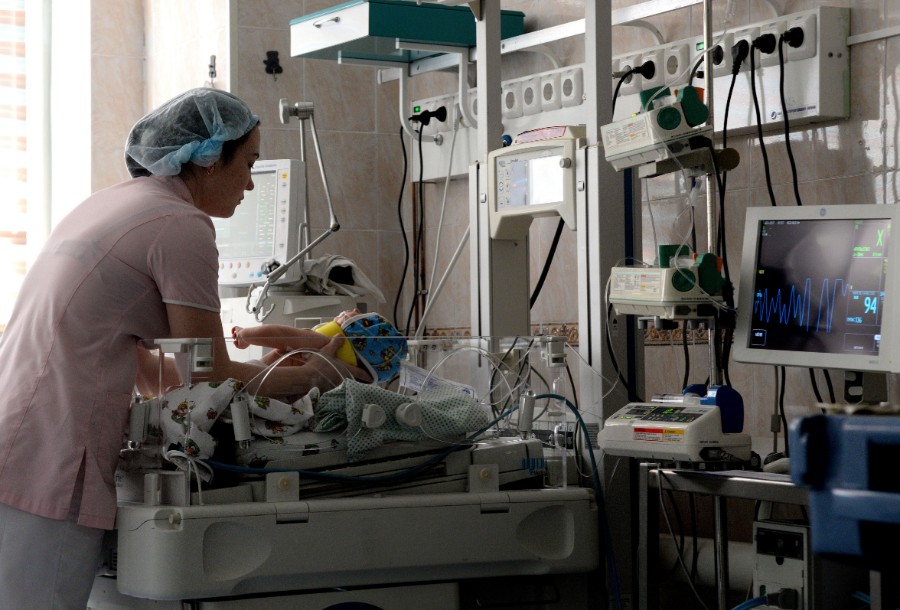 Фото: Игорь Онучин/РИА Новости
Фото: Игорь Онучин/РИА Новости
Зачем проводить скрининг заболеваний у новорожденных?
«Смысл скрининга — выявить заболевание на доклинической стадии — до начала симптомов — и назначить лечение, чтобы или полностью нивелировать все клинические проявления, или сделать их минимальными», — говорит Екатерина Захарова, заведующая Лабораторией наследственных болезней обмена веществ и Лабораторией селективного скрининга, председатель экспертного совета Всероссийского общества орфанных заболеваний.
Сейчас в РФ проводится массовый неонатальный скрининг новорожденных на пять наследственных заболеваний:
- фенилкетонурию — наследственное нарушение метаболизма аминокислот (фенилаланина), которое может привести к тяжелому поражению центральной нервной системы и серьезным умственным нарушениям. При своевременной диагностике и лечении можно полностью избежать патологических изменений;
- врожденный гипотиреоз — группа заболеваний щитовидной железы. Раннее выявление этого заболевания позволяет избежать тяжелой умственной отсталости, задержки физического развития;
- врожденную гиперплазию коры надпочечников, или адреногенитальный синдром, — это группа нарушений, связанных с избыточной секрецией гормонов коры надпочечников. В особо тяжелых случаях происходит нарушение водно-солевого баланса, полиорганная недостаточность;
- муковисцидоз — редкое заболевание, которое поражает дыхательные пути, желудочно-кишечный тракт, печень, экзокринные железы и половую систему. При раннем выявлении заболевания значительно снижается риск осложнений, возрастает продолжительность жизни;
- галактоземию — наследственное нарушение обмена углеводов. При этом заболевании в организме ребенка постепенно накапливаются токсические метаболиты, которые приводят к тяжелой интоксикации. Необходимо как можно раньше начать специализированное лечение.
Скрининговую программу в регионе утверждает местный минздрав. В Москве с 2018 года неонатальный скрининг расширили до 11 заболеваний, в него включили еще шесть нозологий. «Дополнительные шесть позиций, которые включили в массовый неонатальный скрининг в Москве в 2018 году, — это заболевания, для которых есть зарегистрированное лечение, — пояснила Захарова. — Но тесты позволяют определить большее количество заболеваний, и расширение массового скрининга новорожденных будет зависеть от того, насколько будет быстро зарегистрировано лечение и в первую очередь лечебное питание».
В Приморском крае проводится скрининг еще на 20 заболеваний, в том числе на такие болезни, как нарушение обмена аминокислот, органических кислот и дефекты бета-окисления жирных кислот. Однако, как заметила Захарова, лечебное питание для группы заболеваний «нарушение окисления жирных кислот» пока не зарегистрировано. «Еще есть органические ацидурии, для них лечебное питание уже зарегистрировано, но в массовый скрининг они пока не входят. При этом надо отметить, что лечение этих заболеваний недорогое — это в основном диетотерапия, витамины в высоких дозах», — заключила она.
«Массовый скрининг новорожденных в РФ отстает от современного мирового уровня и по числу скринируемых заболеваний, и по применяемым лабораторным технологиям, и по проведению подтверждающей диагностики, и по информированию общества, и по организации помощи семьям с выявленными заболеваниями», — признает директор ФГБНУ «МГНЦ», главный внештатный специалист по медицинской генетике Минздрава России Сергей Куцев.
МАССОВЫЙ СКРИНИНГ НОВОРОЖДЕННЫХ В РОССИИ ОТСТАЕТ ОТ СОВРЕМЕННОГО МИРОВОГО УРОВНЯ
В США в каждом штате неонатальный скрининг проводится в среднем на 40 наследственных заболеваний. В Германии в 1991 году скрининг был расширен с пяти до 30 заболеваний, во многих странах Европы, Южной и Северной Америки скрининги проводятся более чем на 20 нозологий, в зависимости от этнической, эпидемиологической и экономической целесообразности.
Можно ли выявлять на скрининге больше заболеваний?
«Сейчас есть возможность провести «идеальный тест» — тандемную масс-спектрометрию, которая позволяет выявить 40 наследственных болезней, у которых существует эффективное лечение, — рассказал Куцев. — Это тысячи детей ежегодно, которые могли бы не просто выжить, но и избежать инвалидности и даже полностью сохранить здоровье. Анализ одного заболевания стоит 50 рублей, а лечение многих заболеваний — это порядка 500 тысяч рублей в год».
Анализ одного заболевания стоит 50 рублей
Специалист по генетике ссылается на исследование, проведенное в США: у 172 пациентов болезнь выявили на неонатальном скрининге, а у 142 — по клиническим симптомам. В первой группе тяжелые исходы болезни были только у 2% пациентов, а во второй — у 42%.
«Чтобы расширить [в России] список заболеваний, входящих в скрининг новорожденных, нужно провести большую работу: центры, которые будут заниматься неонатальным скринингом, должны быть оборудованы специальными приборами — тандемными масс-спектрометрами, специалисты должны пройти дополнительное обучение», — перечислила Захарова.
Эксперт подчеркнула, что процесс диагностики уже налажен, но придется уменьшить сроки скрининга: сейчас он проводится на четвертые сутки, а если заболеваний будет больше, то лучше проводить его раньше, на вторые сутки. Это связано с тем, что некоторые заболевания могут проявиться в первую неделю жизни и необходимо как можно раньше поставить диагноз.
Захарова считает, что любая скрининговая программа — это нагрузка на бюджет, но если говорить о перспективе на пять-десять лет, то в конечном счете государство получает экономическую выгоду. «Если этим детям вовремя, то есть очень рано, поставлен диагноз и начато лечение, то они не будут отправляться в отделения реанимации, не будет частых госпитализаций в больницы для поиска диагноза и лечения. Например, фенилкетонурия: да, скрининг стоит определенных средств, но эти дети не становятся инвалидами, у них не развивается умственная отсталость, они живут как обычные люди, только на специальной диете», — пояснила она.
Скрининг на фенилкетонурию был начат в 1993 году, за это время в стране родилось примерно 15 тысяч детей с таким диагнозом. Сейчас многие из них создали свои семьи и в этих семьях родились здоровые дети, утверждает эксперт.
Куцев уверен, что необходимо расширить перечень заболеваний для неонатального скрининга по крайней мере до 30. «Мы очень надеемся, что правительство в перспективе примет решение о расширении массового скрининга. Потому что современные технологии, которыми владеет, в частности, Медико-генетический научный центр, уже сегодня позволяют расширить скрининг до 30 наследственных болезней, — подчеркнул он. — Я не устаю повторять, что расходы на скрининг — это небольшие деньги по сравнению с тем, что государство тратит на содержание инвалидов. Если мы сейчас выявляем около тысячи детей, которые сохраняют свое здоровье в результате неонатального скрининга на пять заболеваний, то внедрение расширенного неонатального скрининга позволит нам спасать в год более двух тысяч детских жизней».
Источник
Пренатальный скрининг: мифы и заблуждения. Первый и второй скрининг при беременности. Ультразвуковой скрининг.
Есть или не есть? А если есть, то что? А надо ли УЗИ в день сдачи крови? Можно ли сдать кровь утром? А через неделю после УЗИ? Что нужно сделать перед скринингом первого триместра? Надо ли сдавать второй скрининг при беременности? А в какие сроки?
В наших клиниках ежедневно десятки женщин проходят скрининги 1 и 2 триместра: делают УЗИ и сдают кровь. И при визите к врачу или в процедурный кабинет озвучивают самые невероятные вопросы и мнения относительно этих исследований.
Правила сдачи анализов крови на скрининг обросли мифами и легендами. Пришло время от них избавиться.
Итак, мифы о подготовке к сдачи крови на биохимический скрининг при беременности (двойной тест, четверной тест, оценка риска гестоза)
1. Сдавать первый скрининг нужно на 12 неделе, плюс-минус 5 дней, а второй — не позднее 18 недели.
Это не так. Сроки для сдачи скрининга — с 11 по 13 недель 6 дней, а второго — с 14 по 20 неделю (оптимально с 16 по 18, но возможно и позже).
2. Сдавать кровь на скрининг можно только утром.
Колебаний биохимических показателей скрининга в течение суток не наблюдается, поэтому специально сдавать утром не нужно. Главное не ранее, чем через 3-4 часа после последнего приема пищи (не употреблять жирное).
3. Перед каждым скринингом нужно проходить УЗИ.
Ультразвуковой скрининг 1 триместра делается перед сдачей крови на двойной тест, а следующее УЗИ — уже с 19 по 21 недели, когда скрининг второго триместра (четверной тест) уже сдан. УЗИ первого триместра с определением ТВП и носовых костей участвует в расчете риска в обоих скринингах.
Некорректны рекомендации на одном из сайтов:
«Кровь не следует сдавать сразу после ультразвукового исследования». В случае со скринингом большая часть женщин сдает кровь сразу после первого УЗИ, чтобы два раза не ездить в клинику.
4. До сдачи крови надо несколько дней соблюдать диету с исключением высокоаллергенных продуктов, в том числе, цитрусов, шоколада и красных фруктах и овощах. В других рекомендациях запрещают пить сладкую газировку и употреблять освежающие пастилки в день сдачи анализа.
Мы не видим причины отказывать себе в этих продуктах при подготовке к скринингу.
5. Не рекомендуется заниматься спортом накануне сдачи скрининга.
Если у Вас есть силы и настроение заниматься физкультурой для беременных — это прекрасно, не надо себе отказывать в этом.
6. Отменить все лекарства за 3 дня до сдачи анализа.
Отменять лекарства во время беременности может только врач. Перед сдачей крови на скрининг делать этого не нужно! А вот указать принимаемые лекарства очень важно для корректной оценки результатов.
7. Нельзя сдавать кровь на скрининг, если вы понервничали или простудились.
Тоже миф. Но мы все равно желаем Вам спокойной, легкой и здоровой беременности!
8. Сдавать кровь можно только в день УЗИ.
Нет, это тоже не так. Сделать УЗИ и сдать кровь важно в указанном диапазоне скрининга. Мы рекомендуем сдавать кровь после выполнения УЗИ, так как при УЗИ устанавливается срок и адекватность развития беременности, а также определяются важные для расчета показатели.
9. Скрининг определяет только синдром Дауна, а мне это неважно.
Показатели скрининга показывают гораздо больше, чем синдром Дауна, да и вообще чем хросомомные аномалии (синдром Эдвардса, Патау и другие). Эти исследования позволяет оценить риск развития серьезных осложнений беременности и вовремя принять меры. Дополненный скрининг первого триместра с PlGF позволяет выявить вероятность гестоза — грозного осложнения второй половины беременности. Читайте: «Лабораторные маркеры гестоза».
10. Если первый скрининг хороший, второй скрининг не нужен.
Это не так. Второй скрининг дополняет первый, в том числе, по выявлению других состояний, которые не определяются в первом скрининге.
11. Если УЗИ хорошее, кровь сдавать не нужно.
УЗИ первого триместра не выявляет 100% хромосомных аномалий, какие-то состояния могут пока быть не видны. Исследование крови может определить патологию, еще не видную на УЗИ.
Итак,
относитесь к рекомендациям со здравым смыслом. Например, среди прочих рекомендаций перед скринингом на одном сайте мы нашли даже такое: «Перед взятием крови желательно исключить прием … оральных контрацептивов». Понятно же, что это просто общие правила, которые скопированы на все анализы. Туда же попали рекомендации про голодание не менее 12 часов.
Перед сдачей скрининга продолжайте вести обычный образ жизни, питаться как обычно, не придумывайте низкоаллергенную некрасную диету, продолжайте заниматься физкультурой для беременных.
В день скрининга тоже можно есть и пить. Не стоит принимать пищу в течение 3-4 часов непосредственно перед сдачей анализа, а также есть жирные продукты. Нет, это не повлияет на результат анализа, но в некоторых случаях может потребовать пересдачи.
Из подготовки самое главное — соблюсти сроки для сдачи скрининга.
Здоровья и легкой беременности!
Все о скрининге

Источник
X Международная студенческая научная конференция
Студенческий научный форум — 2018
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке «Файлы работы» в формате PDF
Введение
Актуальность
Неонатальный скрининг (скрининг новорожденных) — это анализ крови, который провести раннюю диагностику приблизительно 50 врожденных заболеваний.
В настоящий момент является самым точным способом ранней диагностики патологий, обусловленных генетической предрасположенностью. По рекомендации ВОЗ неонатальный скрининг включен в перечень обязательных медицинских тестов для детей.
Цели и задачи работы
Цель работы: изучение значения неонатального скрининга для современной врачебной практики
Задачи:
Рассмотреть механизм проведения скрининга новорожденных.
Выявить степень применимости скрининга в качестве метода вторичной профилактики наследственных патологий.
Понятие скрининга новорожденных
Неонатальный скрининг — медицинская диагностическая технология сплошного безвыборочного лабораторного обследования всех новорожденных на некоторые заболевания обмена веществ, призванная обеспечить своевременное выявление и начало лечения больных детей с целью предотвращения их инвалидизации.
В России в течение последнего десятилетия реализуются программы неонатального скрининга двух заболеваний: фенилкетонурии и врожденного гипотириоза. Во многих странах осуществляется сплошное обследование новорожденных на более широкий спектр заболеваний: муковисцидоз, галактоземию, адреногенитальный синдром, болезнь кленового сиропа, дефицит биотинидазы, гемоглобинопатии.
Технология проведения неонатального скрининга
Проведение неонатального скрининга на наследственную патологию основано на определении дефектов ферментов, участвующих в обмене белков и углеводов, в сухом пятне крови на специальной фильтровальной бумаге (тест-бланке). Эти исследования проводят в медико-генетической консультации (центре), куда направляются образцы крови новорождённых одновременно на фенилкетонурию, врождённый гипотиреоз, адреногенитальный синдром, галактоземию, муковисцидоз.
Обязательным условием точности диагностики является тщательная пропитка кровью пятна на тест-бланке.
Забор образцов крови новорождённым в роддоме, в отделении выхаживания недоношенных или патологии новорождённых в детских больницах осуществляется специально подготовленной медсестрой. Кровь берут из пятки новорождённого через 3 ч после кормления: у доношенного ребёнка — на 4-й день жизни, у недоношенного — на 7-й день.
Значение неонатального скрининга
Из нескольких тысяч наследственных заболеваний фенилкетонурия, муковисцидоз, галактоземия, адреногенитальный синдром и врожденный гипотиреоз относятся к таким патологиям, при которых своевременно начатое лечение способно предотвратить развитие тяжелых проявлений заболевания и глубокую инвалидизацию. Причем, чем раньше начато лечение, тем благоприятнее прогноз для течения болезни и для жизни больного ребенка. Частоты этих заболеваний в различных популяциях колеблятся в пределах от 1:2000 до 1:20000, то есть это достаточно распространенные заболевания.
Все это послужило основанием для введения на государственном уровне во многих странах, в том числе и в России, неонатального скрининга для выявления среди новорожденных детей с повышенным риском каждой из этих пяти патологий.
Скрининг на фенилкетонуриию является частью общего скрининга на гиперфенилаланинемию. Он проводится в несколько этапов.
В ходе первого диагностического этапа, возможно использование качественных тестов на повышение концентрации фенилаланина в моче (проба Феллинга и проба с 2,4-динитрофенилгидразином) или в крови при помощи микробиологического теста Гатри. Однако на современном уровне чаще применяют флюориметрический метод, позволяющий быстро и точно определить повышение концентрации фенилаланина в образце крови обследуемого ребенка.
На уточняющем этапе проводится повторное обследование всех детей из группы риска, и далее повторяется исследование на содержание фенилалалнина в крови с использованием аминокислотного анализатора. При концентрации фенилалалнина в сыворотке крови > 15мг%, предполагается диагноз фенилкетонурии, а при концентрации 6-15мг% — гиперфенилаланинемии. При положительных тестах ребенку сразу назначается безфенилаланиновая диета, на основании эффективности которой планируются мероприятия по уточнению диагноза и выбору дальнейшей тактики необходимого лечения.
На заключительном этапе проводится дифференциальная диагностика наследственных гиперфенилаланинемий, и в первую очередь фенилкетонурии, с помощью молекулярно-генетических методов. Если при этом не удается выявить мутаций в гене фенилаланингидроксилазы PAH, проводится измерение активности этого и других ферментов, участвующих в метаболизме фенилалалнина. Исследование проводится в лейкоцитах, фибробластах, а затем и в гепатоцитах, полученных путем биопсии, на фоне пероральной нагрузки фенилалалнином. Определяется содержание птеринов в моче.
При скрининге новорожденных на муковисцидоз в качестве теста используют уровень неонатального иммунореактивного трипсина (ИРТ) в сыворотке крови, концентрация которого при муковисцидозе выше нормы, то есть составляет более 70 нг/мл. У детей группы риска повторно исследуют уровень ИРТ и проводят определение содержания хлоридов в поте (специфический тест на муковисцидоз). Если эти тесты оказываются положительными, назначается ДНК-диагностика. Диагноз муковисцидоза считается доказанным, если удается идентифицировать мутации в гене CFTR.
Отметим, что в тех случаях, когда мутации не удается обнаружить, диагноз муковисцидоза не может быть исключен только на этом основании, так как у больного может быть редкая мутация, которую невозможно идентифицировать в условиях той лаборатории, в которой проводилась ДНК- диагностика.
Группа риска детей с адреногенитальным синдромом выявляется по исследованию в образце крови 17-гидрооксипрогестерона (17-ОНР). Пороговая цифра концентрации этого белка составляет 30 нмоль/л. При таком показателе и выше исследование повторяется, а также выполняется ДНК-диагностика.
Для выявления галактоземии в предоставленном в лабораторию образце крови новорожденного исследуют содержание общей галактозы (галактозы и галактоза-1-фосфата). Результат скрининга можно считать отрицательным при уровне галактозы ниже 400 мкмоль/л (7,2 мг/дл).
Окончательный диагноз галактоземии устанавливается только после детального исследования активности ряда ферментов, обусловливающих нормальный обмен галактозы, и проведения молекулярно-генетического исследования.
Врожденный гипотиреоз это гетерогенная группа моногенных и мультифакториальных заболеваний. Болезнь дебютирует еще в периоде внутриутробного развития ребенка из-за поражения щитовидной железы, в частности, недостаточности тиреотропных гормонов, прежде всего, циркулирующего тироксина. Ведущими причинами нарушения функции щитовидной железы могут быть метаболические дефекты, обусловленные генетическими нарушениями, воспалительные процессы в самой щитовидной железе, применение беременной повышенных доз тиреостатических препаратов. При дефиците продуктов щитовидной железы замедляются окислительные процессы, основной обмен и теплообмен. В частности, нарушается обмен мукополисахаридов, в результате чего в тканях накапливается большое количество креатинина и муцинозного вещества, приводящих к слизистому отеку — микседеме. Следствием всех этих процессов является отставание нервно-психического и физического развития ребенка. Однако при раннем назначении больным гормонов щитовидной железы, в частности, тироксина можно предотвратить развитие инвалидизирующей симптоматики и значительно улучшить состояние больного.
Тяжелая форма врожденного гипотиреоза регистрируется сразу после рождения ребенка. Больной ребенок отличается от сверстников присутствием микседемы, брадикардии, пупочной грыжи, повышенной сухостью и ломкостью волос, вялостью и сонливостью. Для больных характерны большая масса тела (более 4000 г), сухость, шелушение и бледность кожных покровов, холодных на ощупь. Голос низкий, «каркающий». При отсутствии лечения отставание психического и физического развития неуклонно прогрессируют, в последующем формируется олигофрения.
Наиболее яркая картина врожденного гипотиреоза проявляется к 4-6- му месяцу жизни, особенно при естественном вскармливании. До этого времени тиреотропные гормоны ребенок получает с молоком матери. Со временем их недостает организму, и у больного регистрируются тяжелые соматические и неврологические нарушения, при этом эффективность лечения снижается. Дети начинают резко отставать в росте, весе, психическом развитии, вяло реагируют на окружающее, перестают узнавать родителей. Все это обусловливает необходимость ранней диагностики заболевания путем биохимического неонатального скрининга.
В качестве основного скринирующего теста используют содержание в образец крови, взятый из пятки ребенка, тиреотропных гормонов гипофиза и гормонов щитовидной железы (тироксина и трийодтрионина). Концентрацию этих гормонов на первом этапе скрининга определяют иммуноферментным методом. Пороговой цифрой уровня тиреотропных гормонов для обследуемых в возрасте от 1 до 7 дней является 20 мкЕд/мл. Уточняющее исследование проводят в 2-недельном возрасте, на этом сроке пороговым значением тиреотропных гормонов является 5 мкЕд/мл и выше. К этому сроку нормализуется большинство временных нарушений функции щитовидной железы, связанных с фетоплацентарной недостаточностью, родовой травмой, функциональной незрелостью, внутриутробной инфекцией и другими экзогенными причинами. Всем детям с повышенными значениями тиреотропных гормонов и низкими значениями гормонов щитовидной железы назначается курс L-тироксина. Они должны находиться на диспансерном наблюдении эндокринолога, как минимум, до 3-летнего возраста, когда может быть поставлен окончательный диагноз врожденного гипотиреоза.
Для проведения неонатального скрининга среди новорожденных используются наборы «Delfia Neonatal hTSH» (Wallac Oy, Финляндия) и «ТТГ-неоскрин» (Иммуноскрин, Россия). Все исследования выполняются в лабораториях медико-генетических консультаций (центров).
Заключение
Эффективность лечения больных фенилкетонурией, муковисцидозом, адреногенитальным синдромом, галактоземией и врожденным гипотиреозом во многом зависят от профессионализма и ответственного отношения к работе как со стороны врачебного и сестринского персонала родильных домов, так и специалистов медико-генетических центров (отделений).
Таким образом, можно сделать вывод, что неонатальный скрининг на современном этапе развития медицинской науки направлен на раннее выявление лиц с патологическими изменениями генотипа и предотвращение развития тяжелых клинических проявлений заболевания. Он является основным методом вторичной профилактики наследственной патологии. Подобные скрининги целесообразно разрабатывать для распространенных болезней с тяжелым течением, приводящим к инвалидизации.
Список литературы
Горбунова В. Н.//Медицинская генетика. — 201. — С. 331 — 336
Зелинская Д.И.// Сестринский уход за новорожденными в амбулаторно- поликлинических условиях. — 2010. — С.176
Гинтер Е.К.//Медицинская генетика. — 2003. — С. 319.
Мутовин Г.Р.// Клиническая генетика. Геномика и протеомика наследственной патологии: учебное пособие. — 3-е изд., перераб. и доп. — 2010. — С.832
Источник